研究领域
活体光学显微成像旨在在体、原位、无创地观察活体生物组织或模式动物体内的(亚)细胞结构并跟踪其功能动态。相比于离体组织切片或贴壁培养细胞等薄样本,活体光学三维显微成像有两大特点,同时也是技术挑战:一是需要具备光学层析(也称深度层析)能力,从而在无需物理切片的情况下实现活体“厚样本”的在体原位三维成像;二是需要足够的四维(三维空间 × 一维时间)时空分辨率,以记录活体样本或模式动物的高通量三维结构与功能动态信息,并有效对抗活体组织运动的干扰。基础生命科学(尤其是神经科学)和精准临床医学的发展,对活体光学层析显微成像方法不断提出新的挑战,具体而言:
从神经元水平解析线虫、果蝇(幼虫)、斑马鱼等自由行为小型模式动物的全脑乃至全身神经活动动态,是理解大脑工作原理、研究神经活动与生物体行为相互作用的关键;然而常见的光学层析荧光显微成像方法在三维体积成像速率(以下简称“体积率”)、低光毒性、样本空间结构等方面尚存在诸多局限,无法满足系统性全脑神经元活动解析与长时程观测的需求。
临床中传统的活检和组织病理学分析——虽然是目前的金标准诊断方法——本质上是一种有创、离体、非实时的观测手段,丢失了组织固有的三维结构与功能动态信息,实时性不足,依然有漏检或误检的风险。发展在体、原位、高通量三维病理学方法,实现“无需切片,胜似切片”的成像效果,从而在提供实时病理学影像信息反馈的同时尽可能保护正常组织,提升诊疗效率和改善患者预后,是未来精准诊疗的重要发展方向。
围绕上述两大方面应用的需求与挑战,本课题组深度整合中国科大的学术与平台资源,广泛开展理工生医交叉科研合作:一方面推进下一代共焦斜光片扫描(swept confocally-aligned planar excitation, SCAPE)显微方法与仪器研究,大幅提升时空分辨率、荧光收集效率、视场大小等核心性能指标,为自由行为模式动物全脑神经元活动的长时程观测提供平台支持。另一方面,针对不同临床科室的诊疗需求与痛点,定制化构建具有创新架构设计的手持式或内窥式、小(微)型化显微(内窥)体积成像探头,为早期病变筛查、光学活检辅助、精微手术导航等临床诊疗应用提供高时空分辨、无创或微创的原位三维病理学影像与诊断信息,推进医工交叉融合研究与转化。
以往研究成果
1. 设计构建了国际首例面向临床原位在体实时三维病理学显微的小型化SCAPE显微镜,在主物镜孔径光阑直径减小2/3、整机占地面积缩小4/5的同时,仍取得了与台式SCAPE设备同等水平的荧光收集效率和三维分辨率(0.81 µm × 1.07 µm × 2.10 µm),实现了仅靠内源性自体荧光的在体大范围全景体积成像。SCAPE显微术的高时空分辨三维体积成像优势能够有效对抗活体组织运动的干扰,有望实现 “无需切片、胜似切片” 的原位在体、大范围、三维病理学显微成像。
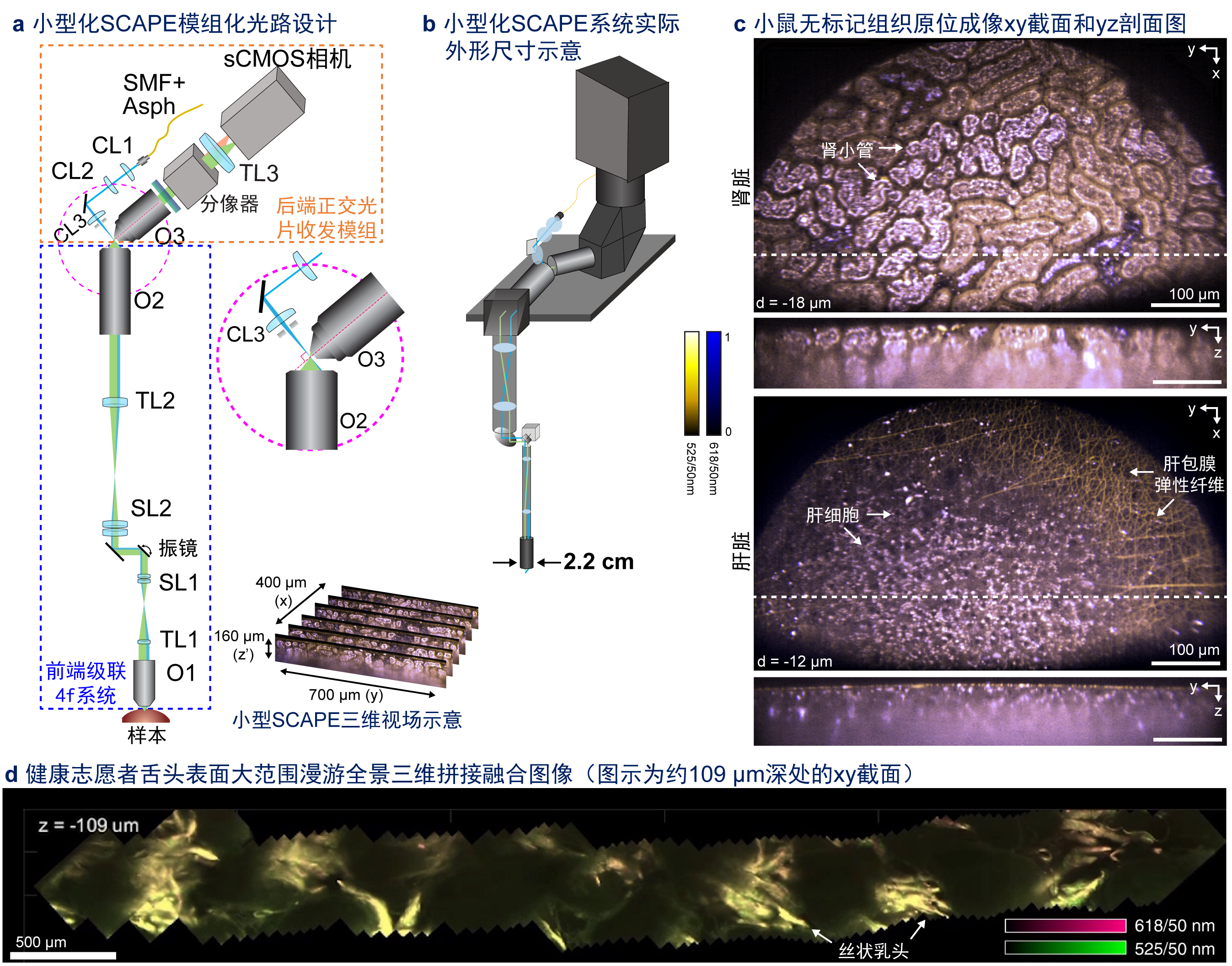
要在临床诊疗场景中应用SCAPE显微成像,一个必备条件是构建相匹配的小型化乃至微型化SCAPE探头。然而标准台式SCAPE显微镜的核心光路高度复杂,为小型化带来了挑战。本人从SCAPE显微术核心原理出发,首先将光片生成透镜组与荧光探测物镜整合为后端正交光片收发模组,避免了台式SCAPE光路所需的二向色镜和分叉光路,显著简化了光路设计;进而设计了桥接第二物镜与主物镜的前端级联4f系统模组,将后端正交光片收发模组的虚拟样品区与主物镜前端的开放样本空间共轭耦合,并通过优化折叠使得前端模组光路更加紧凑(如下图a-b所示)。
动物实验表明,该小型SCAPE显微镜能够仅靠自体荧光清晰可视化肝、肾等小鼠器官组织的细胞级微观结构(如下图c所示);在健康志愿者无标记的舌头上仅需6.4毫瓦激发功率便能取得4.8体积/秒的三维体积率,且在志愿者自由伸缩舌头时,能够从所得的高速“三维体数据流”中直观而准确地估计出相邻体数据块之间的三维位移,进而经配准融合生成覆盖若干毫米范围的三维全景拼接图像(下图d)——由此验证了该小型SCAPE显微镜对活体组织运动出色的抗干扰能力和临床应用潜力。(更多阅读:“无需切片、胜似切片”:中国学者开发小型化在体实时三维显微成像设备)
2. 主导研发了两代基于柔性光纤扫描的微型双光子显微内窥成像技术
2.1. 系统深入地研究了制约双光子显微内窥镜成像信噪比的关键因素,并研究提出了相应的解决方案:
(1) 阐明了长期被忽略的背景噪声——常规掺锗纤芯在激发光脉冲作用下的非线性发光,并利用基于无掺杂纯硅纤芯的定制双包层光纤将非线性背景噪声降至市售双包层光纤的1/4以下;
(2) 建立了双光子内窥镜的后向荧光收集模型,指导优化了定制微型GRIN 物镜的色差补偿和定制双包层光纤内包层的光学扩展量,使荧光收集效率提升了约2.5倍;
(3) 发展了非线性时频联合色散补偿理论与方法,克服了自相位调制效应导致的脉冲频谱压缩,将双光子激发效率相比于传统的线性补偿方法提升了2~3倍。
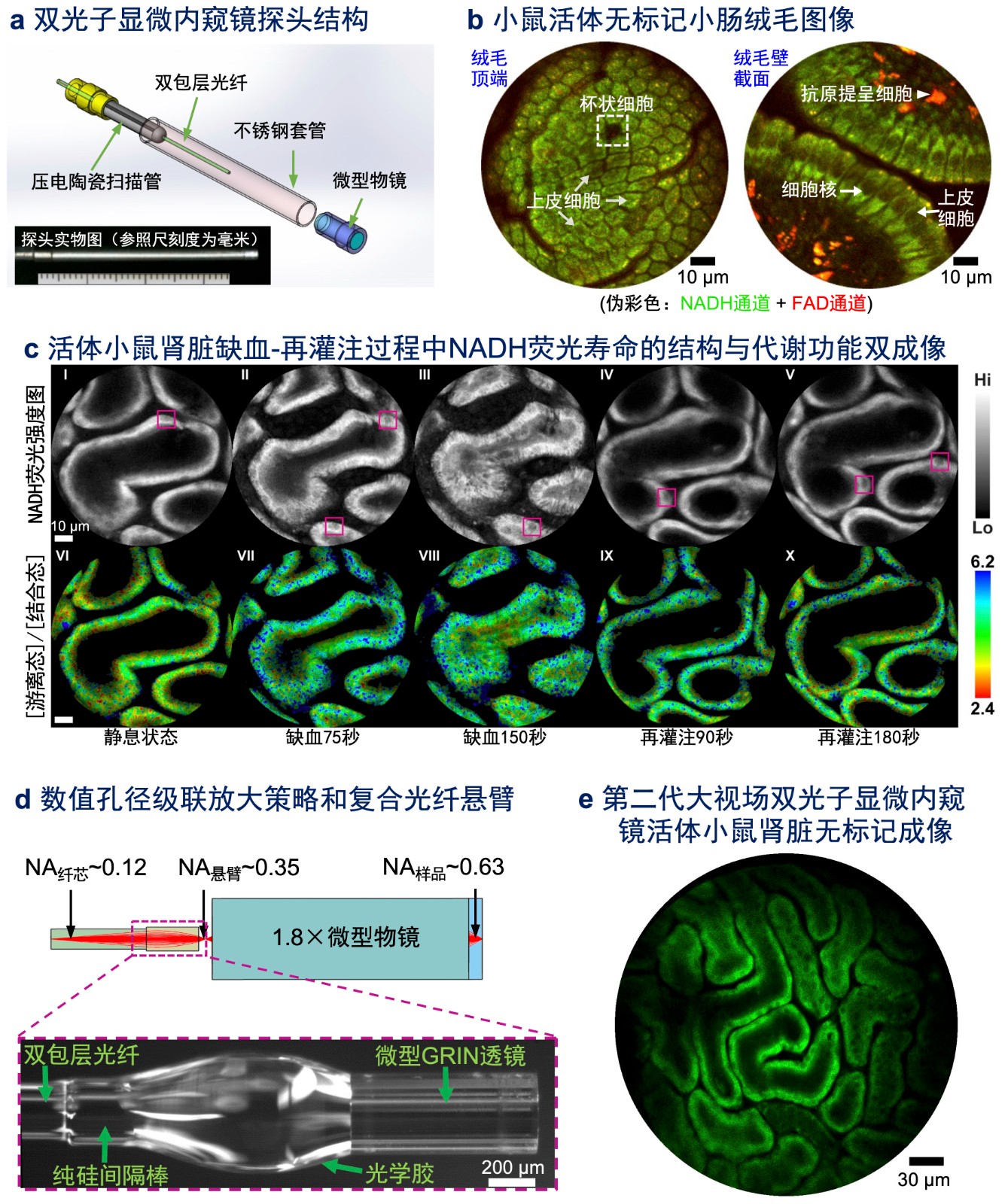
综合上述原理与架构创新,构建了直径仅2.2毫米的“第一代”微型双光子显微内窥探头(见下图a),将探测灵敏度相对于此前设计提升了20倍以上,突破了长期制约光纤双光子内窥技术的成像信噪比瓶颈,实现了可实用的活体无标记实时双光子内窥显微成像(见下图b)。
2.2. 提出了数值孔径级联放大的设计策略,显著提升了第二代光纤扫描双光子显微内窥镜的空间-带宽-成像速度三重积:从理论上论证了光纤共振扫描显微探头的空间-带宽-速度三重积正比于悬臂出射NA的平方;进而创新提出NA级联放大的设计策略,并利用现成光学元件构建了出射NA ~ 0.35的单模复合光纤悬臂(见下图d),打破了传统单模光纤NA约为0.12的物理限制。由此研制了空间-带宽-成像帧率乘积显著提升的“第二代”双光子显微内窥镜,在保证同等分辨率和双光子激发效率的前提下,能够实现:(1) 速度不变、视场直径扩展3倍(空间带宽积扩展约9倍;见下图e),或 (2) 视场直径扩展1.5倍、成像帧率提升3倍,验证了NA级联策略的可行性与灵活性。
2.3. 发展了能同步采集光学氧化还原比和NADH荧光寿命的无标记双光子显微内窥代谢成像方法,首次展示了在活体动物模型上的内窥式双光子无标记结构与代谢功能双成像:深入研究了背景光子的到达时间分布和NADH荧光的弱光子流特性,发展了基于最大似然估计的双指数拟合算法,显著改善了数据分析的准确率,实现了对游离态NADH和结合态NADH的区分定量表征。动物实验表明,该系统能够跟踪活体小鼠皮质肾小管上皮细胞在缺血-再灌注过程中氧化还原比的动态变化和胞内游离态NADH与结合态NADH的丰度涨落(如下图c所示),以及小鼠皮下移植肿瘤细胞在诱导凋亡过程中胞内游离态和结合态NADH的丰度和荧光寿命的变化。
参考文献
Jiapeng Zhu*, Haoliang Luo*, Hanxiao Chen, Yuanhao Zhang, Zixian Cao, and Wenxuan Liang†. A general framework for vectorial detection PSF analysis for oblique plane microscopy utilizing trans-medium intermediate image coupling. Micron (2026). https://doi.org/10.1016/j.micron.2026.104059
Zixian Cao, Jiapeng Zhu, Cheng Zhang, Qianqian Wang, Yankan Huang, Wei Liu, Bingxin Shen, Yuming Chai, Zhaomin Zhong, Li He, Quan Wen, Han Wang, and Wenxuan Liang†. Mesoscopic SCAPE Microscope with a Rescanned, Super-oblique Illumination Plane. bioRxiv 2025.04.25.650616. doi: https://doi.org/10.1101/2025.04.25.650616
Bingxin Shen, Zixian Cao, Yankan Huang, Jiapeng Zhu, Haiyan Huang, Wenxuan Liang†; Computationally designing a dual-aspheric compound lens toward multi-depth endomicroscopy imaging. Applied Physics Letters 126 (22), 223701 (2025). https://doi.org/10.1063/5.0268424
Liang W†, Liu Y, Guan H, Sakulsaengprapha V, Luby-Phelps K, Mahendroo M, and Li X. Cervical Collagen Network Porosity Assessed by SHG Endomicroscopy Distinguishes Preterm and Normal Pregnancy — a Pilot Study. IEEE Transactions on Biomedical Engineering 72(2), 777-785 (2025) †Correspondence DOI: 10.1109/TBME.2024.3472015
Hall G*, Liang W*†, Bhujwalla ZM, and Li X†. SHG fiberscopy assessment of collagen morphology and its potential for breast cancer optical histology. IEEE Transactions on Biomedical Engineering 71(8), 2414-2420 (2024). *Equal contribution, †Correspondence DOI: 10.1109/TBME.2024.3372629
Liang W, Chen D, Guan H, Park HC, Li K, Li A, Li MJ and Li X. Label-Free metabolic imaging in vivo by two-photon fluorescence lifetime endomicroscopy. ACS Photonics 9(12), 4017-4029 (2022) https://doi.org/10.1021/acsphotonics.2c01493
Patel KB, Liang W, Casper MJ, Voleti V, Zhao HT, Perez-Campos C, Liu JM, Coley SM, and Hillman EMC. High-speed light-sheet microscopy for the in-situ acquisition of volumetric histological images of living tissue. Nature Biomedical Engineering 6, 569-583 (2022) https://doi.org/10.1038/s41551-022-00849-7
Liang W, Park HC, Li K, Li A, Chen D, Guan H, Yue Y, Gau YT, Bergles DE, Li MJ, Lu H, and Li X. Throughput-speed product augmentation for scanning fiber-optic two-photon endomicroscopy. IEEE Transactions on Medical Imaging 39(12), 3779-3787 (2020) https://doi.org/10.1109/TMI.2020.3005067
Li K*, Liang W*, Yang Z, Liang Y, and Wan S. Robust, accurate depth-resolved attenuation characterization in optical coherence tomography. Biomedical Optics Express 11(2), 672-687 (2020) *Equal contribution https://doi.org/10.1364/BOE.382493
Voleti V, Patel KB, Li W, Campos CP, Bharadwaj S, Yu H, Ford C, Casper MJ, Yan RW, Liang W, Wen C, Kimura KD, Targoff KL, and Hillman EMC. Real-time volumetric microscopy of in vivo dynamics and large-scale samples with SCAPE 2.0.
Nature Methods 16(10), 1054–1062 (2019) https://doi.org/10.1038/s41592-019-0579-4Li K, Liang W, Mavadia-Shukla J, Park HC, Li D, Yuan W, Wan S, and Li X. Super-achromatic optical coherence tomography capsule for ultrahigh‐resolution imaging of esophagus. Journal of Biophotonics 12(3), e201800205 (2019) https://doi.org/10.1002/jbio.201800205
Liang W*, Hall G*, and Li X. Spectro-temporal dispersion management of femtosecond pulses for fiber-optic two-photon endomicroscopy. Optics Express 26(18), 22877-22893 (2018) *Equal contribution https://doi.org/10.1364/OE.26.022877
Liang W, Hall G, Messerschmidt B, Li MJ, and Li X. Nonlinear optical endomicroscopy for label-free functional histology in vivo.
Light: Science and Applications 6, e17082 (2017) https://doi.org/10.1038/lsa.2017.82
